Физика
Новости физики
Новости науки 29.06.02. Белок NFAT может способствовать расселению раковых клеток в организме.
Белок NFAT (от англ. Nuclear Factor of Acivated T-cells), наряду с другими ДНК-тропными (т.е. связывающимися с ДНК, см. рисунок) молекулами важен для нормального функционирования иммунной системы. Однако предварительные результаты исследований, проведенные в Гарвардской Школе Медицины (Harvard Medical School, HMS) в Бостоне, свидетельствуют, что данный белок имеет свою "темную сторону", облегчая распространение раковых клеток по организму. Данный процесс может приводить к появлению метастазов и прогрессии опухоли.
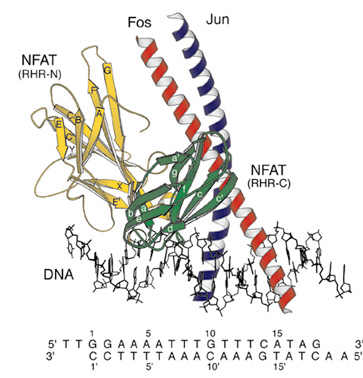
Взаимодействие ДНК - связывающих белков NFAT и AP-1 (последний состоит из двух протеинов: Fos и Jun) с ДНК. Различные участки NFAT отмечены желтым и зеленым цветом.
По словам автора исследования доктора Алекса Тоукера (Alex Toker), ассистента кафедры патологии в Гарвардской Школе Медицины, данная находка может в будущем привести к разработке нового терапевтического подхода в борьбе с раком молочной железы, кишечника и, возможно, других органов.
Протеин NFAT был обнаружен в неожиданно высоких концентрациях в клетках рака груди и кишечника. Чтобы выяснить возможное участие NFAT в процессе опухолевого роста и распространения, ученые из HMS разработали in vitro (т.е. в лаборатории, а не на живом организме) модель клеточной стенки кровеносного сосуда, через который клетки рака должны проникнуть, чтобы заселить другие органы. На этой модели они исследовали, как ведут себя клетки с различным содержанием белка NFAT. Оказалось, что те клетки рака груди, в которых содержание NFAT было высоким, проникали сквозь тканевой барьер, те же, у которых концентрация NFAT была понижена с помощью генной инженерии, были неспособны к проникновению.
Тоукер поясняет, что NFAT в этом случае "способствует миграции раковых клеток и их внедрению в ткани других органов", однако механизм, с помощью которого он осуществляет этот эффект, остается неясным. Дело в том, что NFAT относится к классу молекул, регулирующих считывание информации (транскрипцию) с определенных групп генов. Таким образом, следующим важным шагом должна стать идентификация тех генов и их белковых продуктов, которые "запускаются" с помощью NFAT и способствуют метастазированию (т.е. образованию метастазов). Важно также подтвердить роль NFAT в росте опухолей на лабораторных животных. Ученые планируют в ближайшем будущем изучить, какое значение имеет этот белок при других типах опухолей.
Доктор Тоукер отмечает, что лишь недавно были найдены свидетельства роли NFAT в нормальном развитии сердечной мышцы. Возможно, этот белок присутствует и в нейронах головного мозга.
На рынке лекарств уже существует препарат (циклоспорин А), блокирующий эффект NFAT в иммунной системе. Он применяется для предотвращения иммунных реакций, приводящих к отторжению чужого органа при пересадке. Доктор Тоукер пояснил, однако, что вряд ли циклоспорин А может быть эффективен в борьбе с раком, так как NFAT действует по-разному в иммунных и опухолевых клетках.
За последнее десятилетие факторы транскрипции, к которым относится и NFAT, привлекают пристальное внимание в связи с пониманием их роли для развития опухоли. Например, при таком гематоонкологическом (опухолевом) заболевании, как миелома (см. новость от 26.06.02 и рисунок к ней), предпринимаются попытки воздействовать на другой белок - NF-kappaB, благодаря которому, как показали авторы исследований [1, 2], опухоль приобретает устойчивость к химиотерапии. Интересно, что мишенью для такого воздействия будут как сами опухолевые клетки, так и клетки стромы костного мозга, без поддержки которых раковые клетки не могут сопротивляться терапии.
2i.SU ©R 2015