Химия
Введение
Как был открыт периодический закон
А было ли все так просто, как рассказывал сам Менделеев? На первый взгляд и в самом деле нет ничего трудного в том, чтобы, написав на отдельных карточках названия элементов, их атомные веса и свойства, расположить их по порядку. Ведь из всех способов, какими можно было бы комбинировать эти карточки, наиболее простой -расположить их в ряд по возрастанию атомного веса начиная с элемента с наименьшим весом.
Это, конечно, первое, что должно прийти в голову каждому. Подметить же закономерность в изменении свойств правильно расположенных элементов не^так уж должно быть трудно. Ведь эти свойства во времена Менделеева были хорошо известны.
В чем же заслуга Менделеева? Давайте условимся на некоторое время забыть все, что нам уже известно о химии, все, что мы успели узнать в школе о периодической системе, вообразим, что мы перенеслись в середину прошлого века и можем знать только то, что знали современники Менделеева. К этому времени было открыто и изучено примерно шестьдесят химических элементов. Свыше тридцати элементов было еще неизвестно, и об их существовании никто тогда и подозревать не мог.
Уже были найдены способы определения атомной массы (но здесь мы будем называть эту величину по-старому - атомный вес, как ее называл сам Менделеев). Измеряли атомный вес еще грубо, с малой точностью, и далеко не для всех элементов правильно. Для химиков времен Менделеева это была еще очень трудная задача. Неверно были определены атомные веса у многих элементов, причем, конечно, об этом тогда тоже никто не подозревал.
Как же должен был бы расположить свои карточки Менделеев? Самый малый атомный вес у водорода (Н), он равен 1. Следующим по порядку был в то время литий (Li). Его атомный вес около 7. За ним шел бор (В) с атомным весом около 11. Далее углерод (С) с атомным весом 12, азот (N) с атомным весом 14, бериллий (Be) с атомным весом тоже 14, затем кислород (О), атомный вес которого равен 16, фтор (F) с атомным весом 19 и т. д.
Следовательно, в 1869 г. любой химик, желая расположить карточки с написанными на них обозначениями элементов, их атомными весами и химическими свойствами по возрастанию атомного веса, должен был бы составить вот такой ряд:
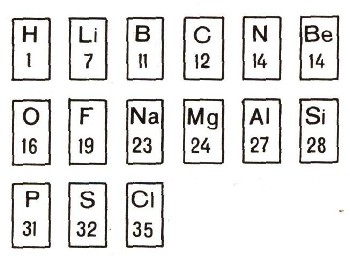
На этих карточках написаны округленные атомные веса с той точностью, с какой они были известны химикам в 1869 г. А как расположил Менделеев свои карточки с элементами? Конечно, на первой карточке у Менделеева также были написаны: название, атомный вес и свойства водорода. Вторую карточку с атомным весом и свойствами металла лития он поместил под карточкой водорода. На третье место рядом с литием Менделеев положил карточку, на которой было написано:

хотя в те времена большинство химиков было твердо уверено (в соответствии со всеми данными химии бериллия), что на этой карточке должно было быть помечено:

Почему же Менделеев, не проводя сам никаких новых исследований, не определяя атомный вес элемента бериллия, не изучая его химические свойства, осмелился исправлять атомный вес - важнейшую и, казалось бы, уже твердо установленную характеристику химического элемента? Ведь он сам никогда не занимался научными исследованиями в области химии бериллия.
На четвертое место Менделеев поместил карточку бора. Пятое место занял у него углерод. На шестом месте - азот, далее следовали кислород и фтор. Девятая карточка, принадлежащая металлу натрию, была им помещена под второй, на которой были записаны химические характеристики металла лития. По порядку следующее место занял магний, за ним - алюминий. Под углеродом оказался кремний, под кислородом - сера, под фтором - хлор. Вот как Менделеев расположил свои карточки с названиями и свойствами элементов в начале своей таблицы:
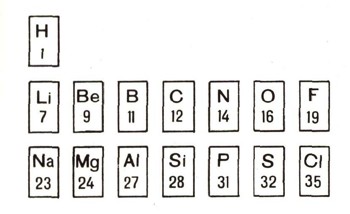
Итак, в вертикальных рядах оказались химически сходные элементы. Металл литий похож на металл натрий: оба мягкие, легко режутся ножом, бурно реагируют с водой, образуя щелочи. Бериллий и магний схожи друг с другом. У фтора много общего с хлором - это едкие удушливые газы, которые образуют с металлами совершенно сходные соединения. И каждый химик знает, что свойства кислорода и серы сходны между собой.
При таком расположении совершенно четко проявилась периодичность свойств у элементов. В двух первых коротких периодах менделеевской таблицы правильно чередуются элементы с аналогичными свойствами. Как же все-таки эти периоды были построены Менделеевым? Пожалуй, он был не прав, когда утверждал, что расположил элементы по их атомному весу.
Если бы он действительно расположил их по возрастанию тех атомных весов, которые были известны науке в то время, то никакого периодического закона обнаружить было бы невозможно даже в первых рядах таблицы. Скорее наоборот, Менделеев установил на основании периодического закона правильный атомный вес бериллия.
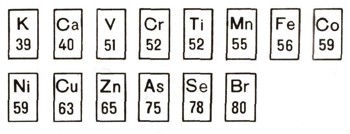
Позднейшие исследования подтвердили это предсказание. Если исходить из атомных весов, известных в середине прошлого века, то следующие два горизонтальных ряда элементов, идущих за хлором, надо было бы построить так:
2i.SU ©® 2015